
DOENÇA DO REFLUXO GASTRO ESOFAGIANO: TRATAMENTO CIRURGICO POR VÍDEO-LAPAROSCOPIA
NILTON CÉSAR ARANHA, NELSON ARY BRANDALISE, ANDRÉ BRANDALISE
INTRODUÇÃO
A doença do refluxo gastroesofagiano (DRGE) é decorrente da falha anatômica e/ou funcional dos mecanismos de contenção da transição esôfago-gástrica. O refluxo pode ser fisiológico ou patológico, sintomático ou assintomático, causar ou não esofagite, e ocorrer na presença ou ausência de hérnia do hiato. O refluxo está relacionado à incompetência do esfíncter esofagiano inferior, ao clareamento esofágico ineficaz, deficiência dos mecanismos de defesa da mucosa esofágica e ao esvaziamento gástrico retardado. A incompetência do esfíncter está relacionada ao baixo tônus pressórico, posicionamento inadequado ( segmento abdominal curto ou ausente) e aos relaxamento transitórios que recentemente foram descritos como o principal mecanismo de refluxo, tanto em indivíduos sadios como em portadores da doença do refluxo. O clareamento esofágico ineficiente resulta da disfunção motora do esôfago e tem como conseqüência exposição prolongada da mucosa ao material refluído, aumentando o dano tecidual. O retardo no esvaziamento do conteúdo gástrico para alimentos líquidos ou sólidos, freqüentemente documentado em doentes com doença do refluxo, aumenta o número de relaxamentos do esfíncter inferior do esôfago que por sua vez aumenta o refluxo.
Os sintomas decorrentes de refluxo são comumente observados na clínica gastroenterológica, sendo que 7% da população geral tem pirose diária e, 29% podem apresenta-la uma vez semanalmente ou ao menos uma vez por mês.
O grau de lesão causado à mucosa do esôfago é dependente da composição do material refluído, do tempo de contato da mucosa, da efetiva capacidade de clareamento, da resistência da mucosa e da capacidade de neutralização pelo bicarbonato salivar.
O tratamento da doença do refluxo gastroesofágico (DRGE) é feito por meio de medidas gerais e dietéticas associadas ou não terapêutica medicamentosa (anti-ácidos, inibidores dos receptores H2, inibidores da bomba de próton e procinéticos).
O tratamento cirúrgico objetiva a interrupção do refluxo patológico através da restauração dos mecanismos de contenção na transição esôfago gástrica. Apesar de definitivo, o tratamento cirúrgico apresenta morbidade operatória, efeitos colaterais e mesmo recidiva tardia entre 2% a 25%.
As esofagogastrofundoplicaturas, são consideradas as formas mais eficazes na contenção do relfuxo gastroesofágico e, portanto, técnicas mais aceitas e aplicadas no tratamento destes doentes.
O surgimento da cirurgia vídeo-laparoscópica e sua aplicação nas doenças do aparelho digestivo na última década, provocou profundas transformações no tratamento de diversas doenças. Aquelas que exigiam amplas laparotomias sem a necessidade de remoção de órgãos tinham indicações cirúrgicas restritas em virtude da grande agressão operatória. A possibilidade de tratá-las de maneira definitiva com reduzido grau de comprometimento da parede abdominal, colocou em maior evidência o novo método cirúrgico.
Desta forma podemos entender a enorme contribuição que a cirurgia vídeo-laparoscópica trouxe no tratamento definitivo da DRGE.
Neste capítulo, os autores discutirão a situação atual das indicações para o tratamento cirúrgico por vídeo-laparoscopia na doença do refluxo e, de forma didática, os tempos operatórios na técnica utilizada pelos mesmos desde 1992, bem como os resultados obtidos.
HISTÓRICO
A primeira operação de gastrofundoplicatura foi descrita por Nissen em 1956. O acompanhamento através de décadas com estudos prospectivos e follow-up clínico cuidadoso, demonstraram tratar-se da técnica mais eficiente na contenção do refluxo gastroesofágico.
Apesar de eficiente, verificou-se que alguns efeitos colaterais ocorreriam, estimulando a modificação da fundoplicatura, originalmente em 360o para fundoplicaturas parciais descritas em 1963 por Andre Toupet, fundoplicatura transtorácica BELSEY (MARK IV) descrita em 1967 por Belsey e Skiner ou ainda fundoplicatura parcial LIND publicada em 1965.
As primeiras séries de doentes com DRGE submetidos a fundoplicatura por vídeolaparoscopia foram publicadas por DALLEMANGNE et al; WEERTS; JEHAES; GEAGEA( 1991). Em 1992, CUSCHIERI publicou os resultados de seus primeiros casos operados à partir de 1989.
A possibilidade de executar por laparoscopia o mesmos tipos de fundoplicatura que se mostraram eficientes pela via laparotômica determinou grande aceitação e aplicação do método na esfera cirúrgica internacional.
m nosso meio, a primeira apresentação de resultados em fundoplicatura laparoscópica foi realizada por AUREO DE PAULA no Congresso Brasileiro de Cirurgia Laparoscópica em São Paulo em 1992. No mesmo ano PINOTTI e col. apresentaram um vídeo de fundoplicatura no XIX Congresso Nacional do Colégio Internacional de Cirurgiões.
Em nosso serviço, no Hospital Centro Médico Campinas, tivemos a oportunidade de introduzir em Setembro de 1992 esta mesma técnica cujos resultados preliminares dos primeiros 50 pacientes foram apresentados em Março de 1994 no IV Curso Internacional de Cirurgia Laparoscópica.
A análise destes resultados iniciais estimulou diversos serviços de Norte a Sul do País a realizar fundoplicaturas laparoscópicas para correção da DRGE.
TRATAMENTO CIRÚRGICO:
INDICAÇÕES
A cirurgia para a correção do refluxo gastroesofagiano está reservada para uma parcela de 5% a 10% dos doentes. São aqueles que apresentam sintomas de esofagite de refluxo por tempo prolongado, recorrente e cujo tratamento clínico, embora bem conduzido, acompanha-se de recidivas dos sintomas, demonstrando ser insuficiente para levar ao tão desejado alívio permanente.
A cirurgia laparoscópica de forma geral é bem aceita pelos pacientes como alternativa definitiva no tratamento da esofagite de refluxo, pela reduzida agressão e rápida recuperação.
Nos últimos anos, com o aparecimento de potentes drogas inibidoras da bomba protônica e medicamentos procinéticos, ambos de atuação bem estabelecida em estudos clínicos controlados, vem-se modificando em parte a maneira de se avaliar e conduzir o tratamento do refluxo. Embora permitam o desaparecimento dos sintomas em curto espaço de tempo, exigem sua utilização permanente por não determinar a cura da doença. Quando o paciente interrompe o uso das drogas pela ausência dos sintomas, o nível de recorrência da esofagite após seis meses é da ordem de 82%.
Diante desta evidência, deve-se considerar que a doença terá caráter evolutivo ao longo dos anos, proporcionando ao paciente os riscos de complicações como estenose ou metaplasia epitelial (Barrett), com seu potencial aumentado para degeneração maligna.
Os critérios para indicar o tratamento cirúrgico são múltiplos e com pequenas variações. Para JAMIESON e DURANCEAU (1988), as indicações são dependentes de das seguintes variáveis:
• estadio I (esofagite não erosiva, refluxo duvidoso, pressão EIE maior que 5mmHg ): tratamento clínico;
• estadio II (esofagite não erosiva, RGE patológico documentado, pressão EIE menor que 5mmHg) tratamento clínico e raramente indicação cirúrgica;
• estadio III (esofagite erosiva, RGE patológico documentado) com sintomas moderados ou intensos : indicação cirúrgica após falha no tratamento bem conduzido;
• estadio IV (estenose ou Barrett) indicação cirúrgica formal.
Para KATADA et al (1995), a indicação cirúrgica mais comum é a falha do tratamento clínico prolongado. Ou seja,
• persistência dos sintomas durante o tratamento adequado;
• recidiva precoce dos sintomas após suspender a medicação;
• não aceitação pelo paciente do tratamento medicamentoso.
Lembra também que a evolução para complicações decorre da falha do tratamento medicamentoso.
Ao nosso ver, deve-se inicialmente ouvir com muita atenção as queixas clínicas do paciente. Entre elas, as mais freqüentes são: queimação epigástrica, retro-esternal e refluxo alimentar, quando em decúbito horizontal ou no esforço abdominal.
Dentre outras considerações como hábito alimentar, atividade profissional, ganho de peso, tabagismo ou etilismo; devemos analisar a idade do paciente, sua condição clínica, o quanto os sintomas têm interferido com sua qualidade de vida e como têm conduzido o tratamento da doença. É obrigatório que saibamos se faz ou não uso de medicamentos apropriados, a duração do tratamento e seus resultados. Somente assim procedendoe iremos compreendendo a real situação vivida pelo doente, e não apenas dados de exames subsidiares.
Após entender o paciente como descrito acima, nos dias de hoje o primeiro exame a ser solicitado para diagnóstico e estadiamento da doença é a Endoscopia Digestiva Alta.
O grau de esofagite presente no momento em que é submetido a endoscopia, é um dado importante mas que não deve ser considerado isoladamente, pois entende-se que se o paciente faz uso freqüente de medicamentos potentes para inibir a produção do ácido ou coibir o refluxo, estaríamos subestimando a gravidade e intensidade da doença.
Informações como dimensão da hérnia hiatal, abertura do hiato diafragmático, aspecto da válvula, perda da visualização dos vasos da submucosa no esôfago distal, sinais de estreitamento do esôfago ou mesmo presença de epitélio de Barrett, devem ser consideradas e relacionadas aos dados clínicos.
Na maioria das vezes, a indicação da cirurgia pauta-se na história clínica confirmada pelo exame endoscópico. No entanto, pode ser necessário em um grupo de doentes a realização de outros exames diagnósticos mais específicos como: pH-metria, manometria esofágica, exame contrastado do esôfago e estômago e ainda a cintilografia esofágica (em crianças) para pesquisa de refluxo gastro-esofágico.
Em crianças ou mesmo em adultos muito sintomáticos que não apresentem esofagite macroscópica e, impossibilitados em realizar outros exames complementares como pH-metria e/ou manometria esofágica, pode-se utilizar o tratamento clínico como teste terapêutico.
A ocorrência de sintomas respiratórios comprovadamente relacionados com DRGE (pneumonias de repetição, bronco-aspirações, crises de asma, tosse noturna, faringites crônicas) são freqüentemente observadas em crianças e corroboram na indicação de tratamento cirúrgico.
Mediante dúvidas, cabe ao cirurgião prosseguir com o estudo do paciente até poder assegurar-se de qual será a melhor forma de conduzir o tratamento.
A indicação inadequada da cirurgia poderá determinar completa insatisfação com os resultados.
Cabe ainda ao cirurgião explicar ao paciente quais serão os prováveis resultados a serem obtidos com a cirurgia a curto, médio e longo prazo; evitando assim desinformações e surpresas desagradáveis.
Assim, podemos sumarizar as indicações de tratamento cirúrgico como:
• esofagites erosivas graus II , III e IV com a presença ou não de hérnia hiatal;
• persistência dos sintomas durante o tratamento adequado;
• recidiva precoce dos sintomas após a suspensão do tratamento;
• não aderência ao tratamento clínico;
• esofagite grau I ou mesmo na ausência de esofagite macroscópica, desde que haja exames que demostrem a existência de refluxo patológico compatível com os sintomas clínicos;
• pacientes jovens com queixas importantes de refluxo e com exames que demonstrem a incompetência do esfíncter inferior do esôfago;
• situações complicadas (refluxo alcalino, Barrett, estenose, grandes hérnias, anemia e etc.)
TÉCNICAS
A cirurgia para o tratamento da DRGE é, ao nosso ver, enganosamente simples, uma vez que o cirurgião precisa estar afeito a inúmeros detalhes técnicos, anatômicos e clínicos para executá-la com sucesso.
As diversas técnicas já descritas para o tratamento desta doença pautam-se basicamente em três linhas gerais: linha anatômica, linha antirrefluxo e linha de inocuidade do refluxo (MALAFAIA e MARCHESINI). Nos dias de hoje observa-se larga aceitação da linha antirrefluxo onde não se objetiva a recomposição anatômica, mas sim utilizar-se do fundo do estômago para confeccionar uma válvula de mecanismo pneumático para contê-lo.
As fundoplicaturas para correção do refluxo, em esofagite não complicadas, realizadas ao longo de muitos anos por laparotomia, se mostraram muito eficientes na contenção do refluxo (>90%).
Nos dias atuais, com a generalização do método videolaparoscópico, houve progressiva redução da via laparotômica, o que nos parece lógico e ético. A técnica para corrigir o refluxo gastroesofagiano por vídeo-laparoscopia apresenta particularidades especiais cujo conhecimento é fundamental para o seu desempenho e desejado sucesso.
O conhecimento e a experiência prévia das técnicas por via laparotômica aliadas à necessária destreza com novos equipamentos e instrumentos utilizados, facilitaram a sua realização.
É perfeitamente possível reproduzirmos pelo método laparoscópico as técnicas de fundoplicatura total (Nissen) ou parciais (Lind, Toupet), que já possuem seus conceitos amplamente divulgados e defendidos por aqueles que sempre as realizavam pelo método laparotômico.
Segundo PETERS e DE MEESTER o principal objetivo do tratamento do refluxo consiste em restabelecer com segurança os mecanismos de contenção da cárdia. Procurar manter a normalidade na deglutição, permitir eructar ou mesmo vomitar quando necessário. A técnica deve restaurar a pressão do esfíncter inferior do esôfago e obtenção de uma extensão de esôfago abdominal não inferior a 3 centímetros. A fundoplicatura deve ser sem tensão, não comprimir o esôfago e estar situada na cavidade abdominal.
Neste capítulo iremos nos referir as técnicas de gastrofundoplicatura laparoscópica já conhecidas e, em especial, a respeito de uma variação tática por nós introduzida que parece cumprir com os objetivos das anteriores e de fácil aplicação.
Apresentaremos a seguir a seqüência e sistematização de eventos por nós recomendados para a boa realização da cirurgia.
ANESTESIA
A anestesia empregada deverá obrigatoriamente ser do tipo geral com entubação endo-traqueal. Para uma realização segura, além dos equipamentos habituais, é necessário a monitorização do paciente com aparelhos de oximetria e capnografia.
O anestesista deverá preocupar-se em manter o paciente todo o tempo curarizado em especial após a abertura da membrana freno-esofágica, pois o aumento súbito da pressão intra-abdominal pode determinar a ocorrência do pneumo-mediastino e enfisema subcutâneo cervical. Esta intercorrência promove aumento da superfície de absorção do CO2 provocando hipercapnia e conseqüente acidose metabólica, elevando os riscos de arritmias.
POSIÇÃO DOS EQUIPAMENTOS, INSTRUMENTOS, PACIENTE E EQUIPE CIRÚRGICA.
O paciente deve ser posicionado em decúbito dorsal horizontal com o membro superior direito junto ao tronco para permitir aproximação do armário com os equipamentos de imagem, insuflação e iluminação. Os membros inferiores deverão estar afastados, estendidos, apoiados em toda a sua extensão sobre perneiras almofadadas e elevados trinta graus em relação ao tronco. Estes cuidados irão facilitar o retorno venoso visando minimizar os riscos de trombose. Lembramos que o retorno venoso dos membros inferiores está já prejudicado devido ao aumento da pressão intra-abdominal e posição de proclive mantidos durante a cirurgia
Os equipamentos acima mencionados deverão estar em armário bem ventilado para evitar hiper-aquecimento e em posição de fácil visualização por todos os componentes da equipe cirúrgica. A instrumentadora deverá estar situada à direita do cirurgião para facilitar a passagem das pinças e auxiliar na introdução delas nos portais.
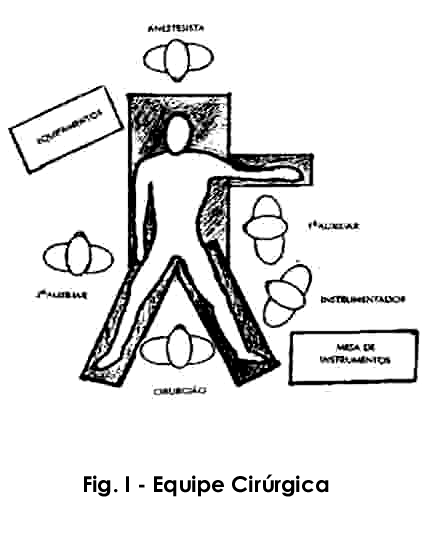
O cirurgião permanece entre os membros inferiores e o primeiro auxiliar a esquerda do paciente. O segundo auxiliar (condutor da camêra) sentado em banco alto situa-se a esquerda do cirurgião e portanto a direita do paciente. Esta situação permite a toda equipe atuar com observação de apenas um monitor. ( figura I ).
O PNEUMO-PERITÔNIO
Para realização do pneumo-peritônio utiliza-se agulha de Verress. O sítio de punção deve variar de acordo com biótipo do paciente, cirurgia proposta, doenças associadas e cirurgias prévias.
A punção habitualmente deve ser realizada através de pequena incisão cutânea transversal situada na linha média ou 2 centímetros a esquerda da mesma e acima da cicatriz umbilical. A distância em relação ao apêndice xifóide varia de acordo com o biótipo, tamanho da hérnia e angulo da ótica a ser utilizada. Costumeiramente este local está situado acima de um ponto intermediário entre a cicatriz umbilical e o apêndice xifóide.
Quando da presença de cicatrizes prévias em abdome superior a agulha de Verress deve ser introduzida no abdome inferior esquerdo, no local onde será colocado o portal para a introdução de instrumento de apreensão e tração do estômago. Somente após a passagem da ótica neste local, é que o cirurgião determinará a necessidade ou não de liberar aderências para colocar os demais portais.
Muitos cirurgiões preferem realizar habitualmente o pneumo-peritônio pela via aberta com visão direta através da utilização de trocarte de Hasson na linha média.
O nível de pressão intra-abdominal deverá ser de no máximo 15 mmHg. A insuflação da cavidade deverá ser inicialmente lenta (1 litro/minuto) para permitir que o anestesista observe as alterações hemodinâmicas dela conseqüentes e possa, em tempo hábil, tratar eventual bradicardia decorrente do reflexo vagal.
OS TROCARTES
A colocação dos trocartes, embora simples, deve ser sempre motivo de preocupação pois acidentes perfurativos podem ocorrer se os cuidados necessários não forem aplicados.
Após obtenção de pressão intra-abdominal desejada (15mmHg), o primeiro portal será colocado para a introdução da ótica. O local deve ser o previamente utilizado na realização do pneumo-peritônio.
O demais locais para introdução dos portais deverão ser definidos e colocados sob visão direta para evitar acidentes. A posição e angulação dos trocartes deve objetivar o favorecimento na realização da técnica cirúrgica.
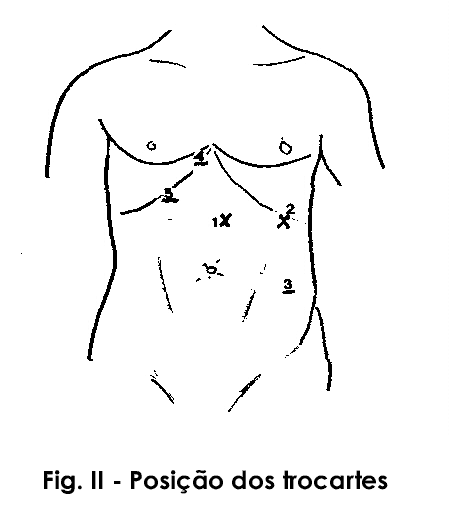
Em nosso serviço temos preferência pela disposição apresentada no esquema (Fig. II) cujas funções seguem abaixo.
• Trocarte 1 (10mm): Para a ótica que será controlada pelo segundo auxiliar.
• Trocartes 2 e 5 (10 e 5mm respectivamente): Permitem a passagem aos instrumentos a serem utilizados pelo cirurgião.
• Trocartes 3 e 4 (5mm): Permitem a passagem aos instrumentos manipulados pelo primeiro auxiliar.
A localização e o diâmetro dos trocartes poderão ser modificados de acordo com as diferentes equipes, biótipo do paciente, preferência do cirurgião e disponibilidade dos instrumentos a serem utilizados. Os trocartes poderão ser metálicos ou descartáveis.
Em situações especiais pode ser necessário a utilização de um sexto trocarte por dificuldade técnica (lobo esquerdo do fígado volumoso, obesidade, re-operações, aderências e cirurgias associadas).
ÓTICAS
A ótica a ser utilizada pode ser de zero grau ou angulada (30o ou 45o) de acordo com disponibilidade e preferência da equipe. Habitualmente as ópticas mais utilizadas são de 10 milímetros, no entanto, também ópticas de 8 ou 5 mm podem ser empregadas, com a desvantagem de fornecerem menor campo visual e iluminação.
Em nosso serviço damos preferência à ótica de 10 mm angulada, pois permite variar a posição de observação, aumentando o alcance visual tão necessário na cirurgia da transição esofago-gástrica.
INSTRUMENTOS
Nos dias de hoje os fabricantes de material cirúrgico se especializaram em produzir instrumentos apropriados que oferecem segurança e facilidade de manipulação. Compete às equipes cirúrgicas selecioná-los e adaptarem-se a sua utilização.
Em nosso serviço utilizamos: bastão palpador como afastador de fígado, dissector reto e curvo de 5mm, pinça atraumática auto estática (apreensão e tração do estômago), pinça com cremalheira de 5mm, gancho de 5mm (dissecção e hemostasia), clipador de 10 mm, tesoura curva de 5mm e porta agulha. Em situações especiais, outros instrumentos poderão ser requeridos, como afastador de pás articuláveis para o fígado, aspirador para possíveis sangramento, etc.
TEMPOS CIRÚRGICOS INTRACAVITÁRIOS:
1) SOLAMENTO DO ESÔFAGO ABDOMINAL, DISSECÇÃO DOS BRAÇOS DO PILAR DIREITO DO DIAFRAGMA E DO FUNDO GÁSTRICO
A apresentação da transição esôfago gástrica é feita pelo auxiliar por meio de um afastador de fígado introduzido pelo portal número 4 e, uma pinça atraumática de apreensão gástrica pelo portal número 3.
No que concerne ao afastador, nossa preferencia é utilizar apenas um bastão palpador de 5mm que permite afastamento cranial do lobo esquerdo do fígado. Alguns serviços preferem a utilização de afastador de 10mm articulado, introduzido no mesmo local em portal apropriado ou então colocado no flanco direito.
A pinça de apreensão gástrica de 5 mm auto-estática ou com cremalheira, deverá permitir uma boa tração e exposição da transição esofago-gástrica, com reduzido trauma à parede do estômago. A utilização de pinça de Babecock de 10 mm pelo mesmo local em portal compatível, é opção preferida por alguns cirurgiões.
O afastamento cranial do fígado e a tração caudal do estômago permite adequada apresentação do ligamento hepato-gástrico e da membrana freno-esofágica. Inicia-se a secção do ligamento acima do ramo hepático do nervo vago utilizando-se para isso de um instrumento tipo gancho (nossa preferência) ou tesoura, sempre ligados ao bisturi elétrico.
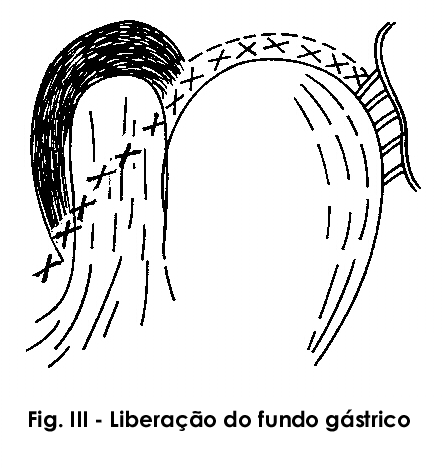
Esta secção continua transversalmente da direita para a esquerda dividindo o peritônio e a membrana freno-esofágica com o devido cuidado de não lesar o nervo vago anterior. À partir do angulo de Hiss a secção da membrana peritonial prossegue junto ao fundo do estômago até o primeiro vaso curto. A liberação das aderências do estômago com o diafragma deverá ser tão ampla quanto necessária para permitir a obtenção de fundo gástrico amplo a ser utilizado na fundoplicatura (Fig. III).
Quando esta liberação atinge a retrocavidade, a parede porterior do fundo gástrico poderá ser facilmente tracionada por detrás do esôfago, permitindo a realização de válvula frouxa. A secção dos vasos curtos para liberação mais ampla do fundo gástrico, realizada rotineiramente por alguns serviços, não nos parece necessária na maioria dos casos. Pode ser necessária em situações especiais como nas re-operações, quando o fundo gástrico apresenta tamanho reduzido ou de difícil mobilização. Nestes casos, a liberação de três ou quatro vasos curtos pode ser feita após ligadura por clips de titânio, cauterização bipolar ou com a utilização do bisturi ultra-sônico.
Uma vez seccionada por completo a membrana e o ligamento, identificamos o braço direito do pilar direito do diafragma e o seguimos até sua inserção na coluna. Isto facilitará a identificação da inserção do braço esquerdo do mesmo pilar. Segue-se com a dissecção do esôfago terminal que pode ser facilitada pela tração do estômago, preocupando-se com a identificação dos nervos vagos. O afastamento do esôfago para o lado esquerdo ou direito é auxiliado pelo bastão, ao mesmo tempo em que este afasta o lobo esquerdo do fígado.
Durante o isolamento do esôfago abdominal pode-se encontrar por vezes a presença de tecido gorduroso exuberante junto ao mesmo, devendo ser removido para melhor individualização da transição esofago-gástrica.
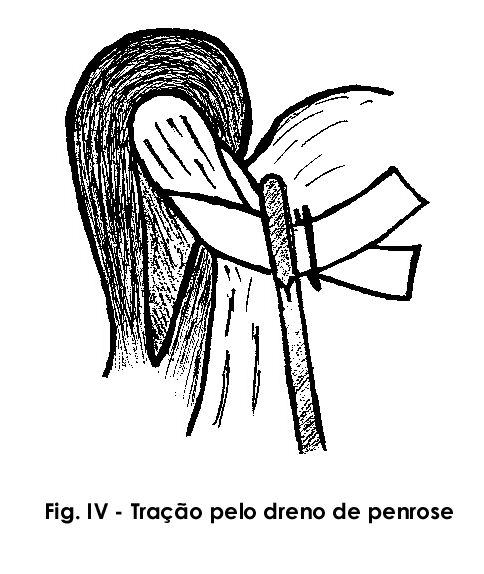
O isolamento do esôfago deve ser amplo o suficiente para proporcionar um segmento abdominal adequado. Para facilitar este tempo, deve-se passar uma gaze na forma de rolo conduzida por pinça romba por detrás do esôfago da direita para a esquerda, sempre acompanhada de visualização clara desta região para evitar a perfuração instrumental do esôfago. Uma vez passada a pinça por trás do esôfago apreendemos um segmento de dreno de Penrose com aproximadamente seis centímetros. As extremidades do dreno deverão ser então reunidas anteriormente ao esôfago e fixadas por pinça tipo cremalheira e clipe. A sua tração permite boa apresentação do esôfago sem grandes riscos de perfuração (Fig.IV).
Na presença de esofagite intensa associada a peri-esofagite, a manobra de dissecção deve se estender cautelosamente em direção ao mediastino em virtude dos riscos de lesão pleural. Esta ocorrência poderá levar a maior grau de dificuldade ventilatória com repercussões gasométricas, porém, em geral não obriga a interrupção do método operatório.
Uma vez o esôfago isolado e os pilares individualizados, completa-se a liberação do fundo gástrico se necessário, para permitir sua passagem sem tensão por detrás do esôfago abdominal. Este teste deve ser realizado rotineiramente antes de iniciar o tempo seguinte (Fig. V).
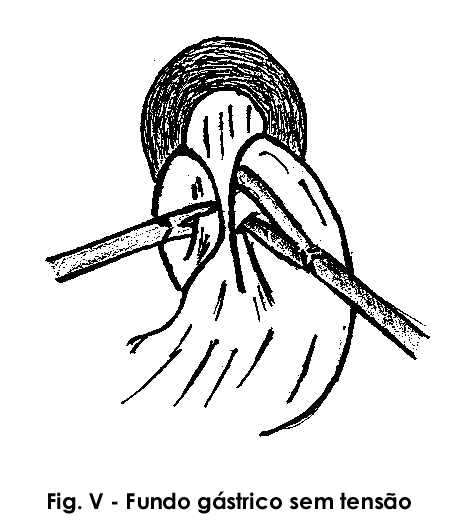
2) APROXIMAÇÃO DOS BRAÇOS DO PILAR DIAFRAGMÁTICO
A sutura para a aproximação dos braços do pilar diafragmático deve ser realizada utilizando-se de fio inabsorvível multifilamentar (00) com agulha de 2,0 ou 2,5 cm curva ou em esqui. Utilizamos sempre o ponto em X com o primeiro nó em dupla laçada para assegurar a sua fixação (Fig. VI).

O número de pontos a serem dados varia de acordo com o grau de afastamento dos braços do pilar. A redução do anel hiatal deve permitir, além do esôfago, a passagem sem dificuldades de uma de gaze. Deve-se ter sempre o cuidado de não apertar os nós em demasia para evitar a isquemia e secção das fibras musculares. Este tempo, segundo alguns cirurgiões, deve ser precedido pela colocação de uma sonda calibrosa (50 a 60 French) oro-gástrica para minimizar os riscos de constricção do esôfago.
Recomendamos a execução apenas de nós internos, que quando bem realizados permitem redução do tempo cirúrgico.
3) REALIZAÇÃO DA GASTROFUNDOPLICATURA
A passagem do fundo do estômago por detrás do esôfago é novamente realizada com o auxilio de duas pinças, uma para tracioná-lo da esquerda para a direita e outra empurrar o fundo gástrico. O primeiro ponto simples ou em X é então realizado envolvendo ambos os segmentos de fundo gástrico em torno do esôfago abdominal.
A válvula pode ser do tipo total ou parcial modificando-se a técnica empregada apenas a partir deste momento.
a)Válvula total 360 graus (NISSEN):
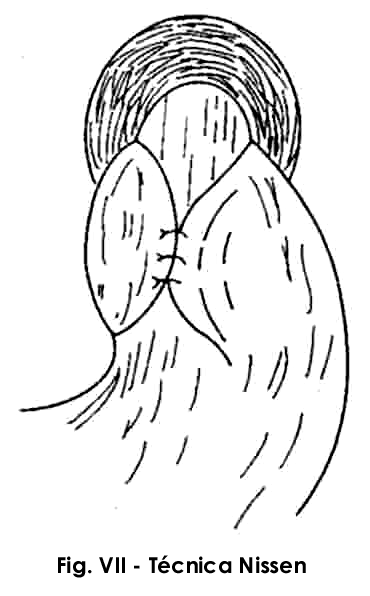
Além do ponto mediano (estômago - estômago) realiza-se mais um ponto acima e outro abaixo fixando ambas as partes do fundo gástrico na parede anterior do esôfago abdominal (estômago - esôfago - estômago). É necessário que este envolvimento seja curto (2 a 3 cm) e frouxo para o sucesso da técnica (Fig.VII).
Nos dias de hoje, a maioria dos cirurgiões que se utilizam desta técnica, evitam válvulas mais extensas como originalmente descrita por este autor (4 a 5 cm).
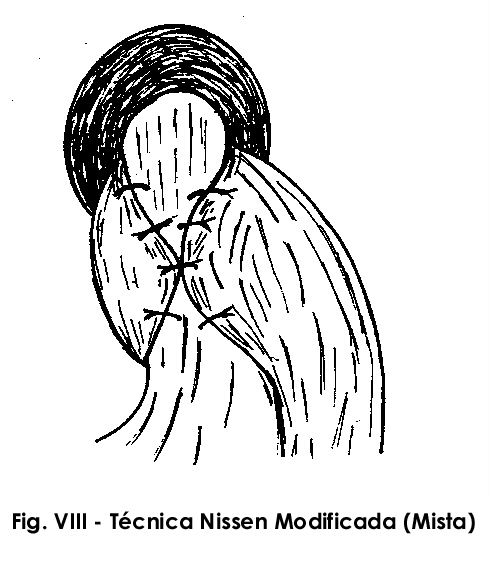
b)Válvula NISSEN modificada (mista):
Além do ponto inicial “estômago-estômago” serão realizados pontos acima e abaixo deste, fixando o fundo gástrico nas superfícies antero-laterais direita e esquerda do esôfago; a semelhança de fundoplicatura parcial. Normalmente um ponto acima e um abaixo são suficientes para a fixação da válvula, porém, se desejarmos ampliar o comprimento da mesma, podemos acrescentar pontos adicionais. Deve-se evitar que a agulha transfixe completamente a parede das vísceras envolvidas (Fig.VIII).
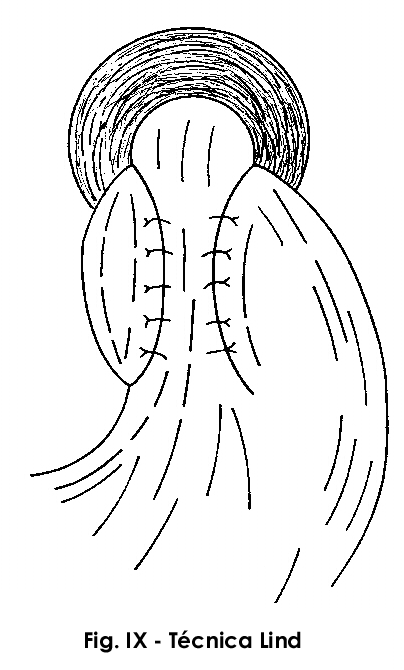
c)Válvula parcial (LIND ou TOUPET):
A realização da válvula tipo Nissen modificada com fundoplicatura parcial mais extensa, seguida da secção do ponto inicial (estômago - estômago) e fixação de ambas as partes do fundo gástrico lateralmente ao esôfago, transforma a técnica em gastrofundoplicatura parcial (Fig.IX).
4) REVISÃO DA HEMOSTASIA E RETIRADA DOS PORTAIS
Realiza-se a revisão da hemostasia com auxílio de pinças e gazes ou mesmo usando um aspirador quando necessário. A retirada dos portais deve ser feita uma a uma, sob observação do orifício por eles determinados na parede abdominal, na tentativa de surpreender possíveis sangramentos nesses locais. O último portal a ser retirado é o do canal de trabalho (número 2) pois permite passagem de instrumentos para o controle de eventual sangramento de parede. Finalmente, retira-se a ótica e o portal da mesma, após esvaziar completamente o gás da cavidade abdominal.
A sutura da aponeurose deverá ser realizada rotineiramente se o portal da ótica transfixou a linha média e quando necessário, nos demais orifícios de 10mm. A sutura nas inscisões de pele é feita com mononylon.
COMPLICAÇÕES DO MÉTODO
Embora as técnicas possam ser realizadas com segurança por equipes adequadamente preparadas, não podemos nos esquecer que complicações podem ocorrer e devem obrigatoriamente ser identificadas e tratadas ainda durante a cirurgia. Os cirurgiões que se iniciam no método estão,naturalmente, mais expostos às complicações.
Complicações ocorrem a partir do momento da realização do pneumo-peritônio ou na introdução do primeiro trocarte (às cegas), como a lesão de vasos ou de vísceras. Estes acidentes quando não identificados, colocam o paciente em sérios riscos de vida. Quando identificados a correção poderá ser feita pelo próprio vídeo-acesso ou por laparotomia.
A perfuração gástric é em especial provocada por tração excessiva ou por uso de instrumentos não apropriados. Mais uma vez a sua identificação permitirá a correção sem conseqüências maiores, no entanto se descoberta apenas no pós operatório, o paciente terá que ser reoperado correndo sérios riscos.
A perfuração esofágica por manipulação inadequada, mais freqüente nos casos de esofagite avançada com estenose, determina conseqüência gravíssima se não identificada e tratada.
A ocorrência de sangramento, mais comum nos casos onde é necessário ampla liberação do fundo gástrico com ligadura de vasos curtos, exigirá da equipe habilidade maior para sua correção, constituindo-se por vezes em motivo para conversão. Felizmente a lesão esplênica com necessidade de esplenectomia é pouco referida.
A conversão para método de abordagem laparotômico no intuito de corrigir complicações ou concluir o ato cirúrgico não deve ser considerada como demérito da equipe, mas simplesmente mudança de tática visando a segurança do paciente. Dificuldades se apresentam em especial quando o lobo esquerdo do fígado é grande e friável, nos grandes obesos, nas grandes hérnias hiatais, múltiplas laparotomias prévias para cirurgias do andar superior do abdome ou mesmo no esôfago curto.
RESULTADOS
Devemos considerar a análise dos resultados em três etapas diferentes: resultados imediatos, a médio prazo e resultados definitivos.
RESULTADOS IMEDIATOS
A ocorrência de vômitos em torno de 20% dos pacientes pode determinar a ruptura ou esgarçamento do pilar diafragmático, ocasionando a recorrência da hérnia. Para evitá-lo aconselha-se o uso de anti-heméticos profiláticos, sendo muito eficaz o uso de 4 a 8 mg de Ondasetron.
Os sintomas de refluxo e azia desaparecem após a cirurgia. O grau de desconforto abdominal no pós operatório imediato é leve e solucionado com analgésicos comuns. Observa-se com alguma freqüência desconforto e mesmo dor nos ombros que pode persistir ainda alguns dias requerendo às vezes uso de anti-inflamatórios.
Os pacientes podem receber alta hospitalar após 12 a 24 horas de observação sempre precedida da reintrodução da alimentação.
A dieta inicialmente deverá ser mantida com característica cremosa durante uma a duas semanas, quando se observa melhora na passagem dos alimentos.
É freqüente a sensação de plenitude pós prandial e incapacidade de eructar nesta fase.
O retorno à atividade laborativa depende do tipo de trabalho executado pelo paciente. Os burocratas em geral reassumem seus afazeres em torno de cinco a sete dias após a cirurgia. O paciente deve ser orientado a evitar esforço físico importante (esportes), em especial exercícios abdominais durante o período de trinta dias.
RESULTADOS A MÉDIO PRAZO
Persistem sintomas de disfagia leve a alimentos sólidos, dependendo da técnica aplicada, durante um período em torno de trinta dias. Estes podem raramente persistir por até três meses, exigindo exame endoscópico, radiológico ou manométrico para melhor entendimento da causa.
Não raro, os pacientes que não conseguem eructar apresentam freqüentemente sintomas de flatulência gerando desconforto e constrangimento.
RESULTADOS TARDIOS
De forma geral em torno de 93% a 96% dos pacientes apresentam completa satisfação com os resultados obtidos com a cirurgia, classificados em Visick I. Uma pequena parcela de pacientes referem benefícios, referindo apenas quando interrogados, com um ou outro sintoma dispético (Visick II).
A persistência ou recorrência da doença raramente ocorre. Os pacientes que apresentam grau de esofagite avançada com estenose no pré-operatório (grau IV) estão mais sujeitos a este acontecimento.
Estes bons resultados tardios obtidos pelos grupos de cirurgiões com experiência no método, se assemelham as grandes séries de pacientes submetidos a tratamento por via laparotômica.
Mediante os bons resultados referidos da análise da literatura nacional e estrangeira, confirmados também com a nossa experiência, concluímos que o método constituiu-se num dos maiores avanços no tratamento da doença do refluxo
BIBLIOGRAFIA
1-ARANHA,NC, BRANDALISE,NA: Tratamento videolaparoscópico da esofagite de refluxo pela técnica "mista"(Nissen modificada). G.E.D. 1995, 5:219,222.
2-BRANDALISE, N.A. & ARANHA, N.C. - Esofagite de refluxo - Tratamento Cirúrgico pela Vídeo-Laparoscopia. Manual de Cirurgia VídeoEndoscópica. Rio de Janeiro, Osmar Creuz, 203-208, 1993.
3-BRANDALISE, N.A. & ARANHA, N.C. - Esofagites de refluxo. Tratamento por vídeo-laparoscopia. Sylabus do IV Curso International de Cirurgia Laparoscópica. Hospital Samaritano, Goiânia: 115-116, 1994.
4-BRANDALISE, N.A & ARANHA, N. C. -Tratamento cirúrgico da esofagite de refluxo por vídeo-laparoscopia - Rev. C.B.C. vol XXIII, 3: 119-122, 1996.
5-BRANDALISE, N.A & ARANHA, N.C. -Doença do refluxo gastroesofagiano - Técnica Operatória. Livro : Doença do refluxo gastroesofagiano - João Batista Marquesini & Osvaldo Malafaia - Clinica Brasileira de Cirurgia - C.B.C. - Ano II - vol. III - Editora Atheneu, 1996.
6-CUSCHIERI, A., SHIMI, S., NATHANSON, L. K. - Laparoscopic redution, crural repair, and fundoplication of large hiatal hernia. The Am. J. Surg. 163: 425-430, 1992.
7-DEMEESTER, T.R., BONAVINA, L., ALBERTUCCI, M. - Nissen fundoplication for gastroesophageal reflux disease. Ann. Surg. 204: 9-20, 1986.
8-DE PAULA, A.L., HASHIBA, K., BAFUTTO, M. - Tratamento laparoscópico da doença do refluxo gastroesofageano. Sylabus do V Curso Internacional de Cirurgia Laparoscopica. Hospital Samaritano, Goiânia: 91-95,1994.
9-GAMA RODRIGUES,J.J.; BRESCIANI,C.;PINTO,P.E.; et al:.- Esofagite de refluxo e hernia do hiato por deslizamento.- Tratamento por video-laparoscopia, Cirurgia video laparoscopica e laparoscopia diagnóstica em aparelho digestivo. Ed. Independente São Paulo pg 126-134,1992.
10- GAMA RODRIGUES, J.J. - Hérnia hiatal por deslizamento. Esofagogastrofundopexia associada à hiatoplastia. Avaliação clínica e funcional. Tese de Livre Docente. Faculdade de Medicina da Univ. de São Paulo. São Paulo, 1974.
11- LIND, J.F., BURNS C.M., MacDOUGALL, J.T. - "Physiological"repair for hiatus hernia - manometric study. Arch Surg. 91: 233-237, 1965.
12-MALAFAIA, O., MARCHESINI, J.B., RIBAS FILHO, J.M. - Refluxo gastro-esofágico. Linhas gerais que norteian as técnicas cirúrgicas. Sylabus do IV Curso Internacional de Cirurgia Laparoscopica. Hospital Samaritano, Goiânia : 69-72, 1994.
13-NISSEN,R.- Gastropexy and fundoplication in surgical treatment of hiatal hernia. Am. J. Dig. Dis.:6:954-961, 1961.
14-PINOTTI, H.W., NASI, A., DOMENE, C.E., SALTO, M.A., LIBANORI, H.J. - Tratamento cirúrgico da esofagite de refluxo pela vídeo-laparoscopia. Apresentado no XIX Congresso Nacional do Colégio Internacional de Cirurgia, São Paulo, 1992.
15-PERDIKIS, G.; HINDER, R.A ; LIND, R.J.; RAISER, F.; KATADA, N. - Surgical Laparoscopy & Endoscopy- 7:17-21- 1997.

 LEIA TAMBÉM:
LEIA TAMBÉM: -
Hérnia de Hiato
Doença do Refluxo Gástrico. -
Hérnias
Inguinal, umbilical e outras. -
Vesícula
Pedra ou pólipos na vesícula. -
Outras Doenças
do Aparelho Digestivo. -
Obesidade/
Diabetes
Saiba mais sobre elas. -
Nutrição
Melhore sua qualidade de vida. -
Biblioteca Médica
Leia artigos e publicações.



